date:2026-05-12 10:08:57
理解神经系统,不只是研究细胞本身,更是解码生物学中最复杂的系统之一。神经元形成动态网络,通过电信号与化学信号持续交流,并与星形胶质细胞、小胶质细胞及周围微环境相互作用。在实验室中重现这种复杂性极具挑战,但对研究神经发育、功能与疾病机制至关重要[1]。
这正是体外模型的价值所在。它能在保留关键生物学行为的前提下,适度简化复杂体系,便于研究者解析特定分子与细胞机制。历经发展,体外模型已从简单的平面培养,演进为高精度3D培养系统、类器官与可控微环境体系[2],不同模型从不同维度揭示神经系统的运行规律。
Flat but Powerful: Why 2D Neuronal Cultures Still Matter
二维神经元培养通常是神经科学研究的起点,这得益于其独特优势:它提供干净、可控的环境,可高精度观察单个细胞及其行为。在2D体系中,神经元在平面基质上生长,便于追踪神经突生长、极性建立与突触形成,同时具备极佳的光学可达性,适用于高分辨率荧光成像、钙成像与活细胞分析[3]。

这种简洁性让研究者可聚焦特定细胞机制,并实现高度定量分析。如今,二维神经元培养已成为自动化成像工作流程的核心,通过高内涵成像和基于人工智能的分析对数以千计的细胞进行分析[4]。经过成像优化的耗材,如(µ-Plate 96 well)96孔培养板和(µ-Plate 384 well)384孔培养板板,以稳定培养条件与可靠光学质量支持这些方法,使检测细微的表型变化更加容易。
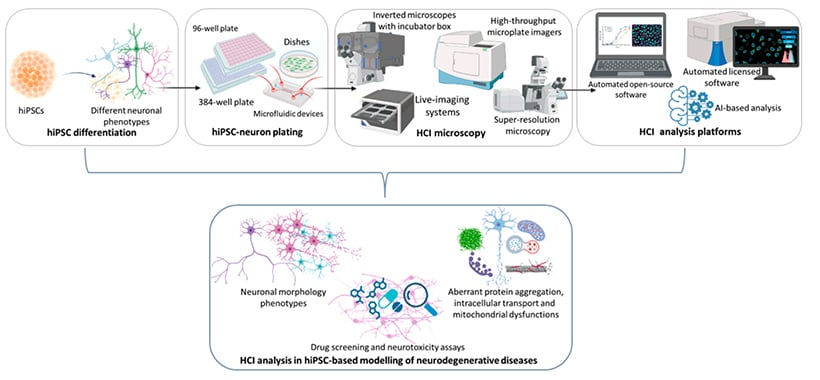
然而,2D培养的神经元仍然缺乏天然组织中的空间背景和机械刺激,这可能影响网络形成、连接和对刺激的响应方式。尽管如此,2D培养仍然是重要的基础,尤其是在精度和可重复性至关重要时。
Stepping into the Third Dimension
从2D到3D的转变,不仅仅是几何形状的改变,更是神经元行为的深刻革新。与在平面上铺展不同,细胞开始在周围的基质中导航,自主决定生长的位置、连接的方式以及网络的稳定。这种三维环境引入了空间约束、局部梯度和机械阻力,所有这些都影响着神经元网络的形成和随时间的演化。
这创造了一个更接近生理的微环境,细胞不仅彼此相互作用,还与周围基质相互作用,从而形成更复杂的网络、改善分化并获得更具生理学相关性的行为。神经球状体(Neural spheroids)是常见的例子,细胞自组织成致密、相互连接的结构,模仿了组织组织的某些方面。
在3D培养系统中,脑类器官代表了更高层次的生物学复杂性。这些系统源自多能干细胞,包括诱导多能干细胞,它们能自组织成类组织结构,具有多重神经细胞类型和区域特异性身份。这些系统使研究者能够在体外重现人类大脑发育和功能的关键方面,从早期模式化到网络形成,并用于研究神经发育障碍、神经退行性疾病以及影响大脑的病毒感染[5,6]。
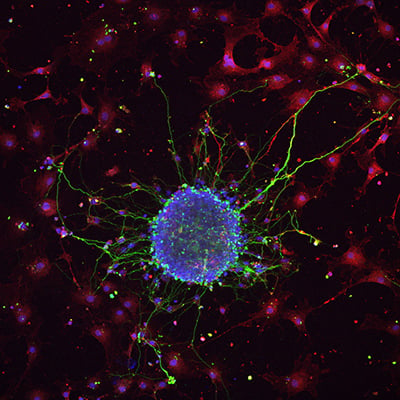
图2.小鼠神经干细胞经视黄酸诱导分化后,在多聚-L-赖氨酸包被玻璃上形成的神经球。神经元用Tuj1染色,星形胶质细胞用GFAP染色,细胞核用DAPI染色。图片提供:Lina Papadimitriou, Anthi Ranella, TERMIM Lab, Institute of Electronic Structure and Laser, Crete, Greece
现代3D系统的强大之处在于,能够将结构复杂性与受控环境相结合。标准化的耗材,如:
• µ-Plate 96 Well 3D(96孔3D培养板):支持高通量环境中实现可重复的凝胶基质实验
• µ-Slide 15 Well 3D(15孔3D培养载玻片):支持受控的基质包埋,试剂消耗量低

When Do Organoids Start to Think?
一个极具吸引力的问题是:细胞团何时从单纯模型转变为具备网络功能的系统?
脑类器官并不具备意识层面的“思考”,但能实现令人瞩目的功能活动:产生自发电活动、形成同步放电节律、构建功能性神经网络。它们并非在思考,而是开始彼此“对话”。
这些早期相互作用,为解析大脑自我构建过程提供独特视角。研究者可实时观察信号如何产生、连接如何稳定、网络行为如何演化,这使得类器官成为活体测试系统,我们可以在其中实时研究功能形成的初步阶段。
同时,类器官也带来了挑战。缺乏血管化限制了营养供应和生长,而样本间的变异性可能影响可重复性。因此,谨慎的操作和稳定的培养条件对于获得一致可靠的结果至关重要。
构建结构只是研究的一部分。要真正理解神经元行为,必须精准调控周围微环境。细胞对流体剪切力、浓度梯度、空间排布等物理与化学信号高度敏感,这些信号决定网络的形成与功能。
在神经系统中,内皮细胞持续处于流体环境中,剪切应力影响细胞形态、信号传导与屏障完整性。体外可控流体体系,可用于研究血脑屏障功能与功能异常机制。

微流控系统可精准调控流体、梯度与营养交换,为原本静态的培养增加动态条件,从而提高生理学相关性[7]。例如:
• µ-Slide I Luer 3D (单通道3D培养载玻片)
• µ-Slide Spheroid Perfusion (球体灌注通道培养载玻片)
等上述平台可将3D培养与受控流动相结合,用于可重复的实验。
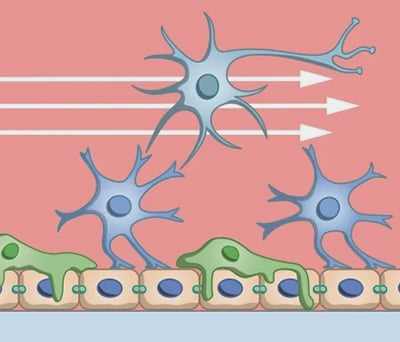
图3.微流控系统中的受控流动引入了剪切应力和梯度,从而在体外实现了更具生理学相关性的细胞行为和血脑屏障功能
微图案技术(Micropatterning technologies)进一步提升神经模型的可控性:通过限定神经元黏附位置与连接方式,引导神经突沿预设线路生长,实现标准化网络构建,用于研究神经连接、信号传递与细胞间相互作用。
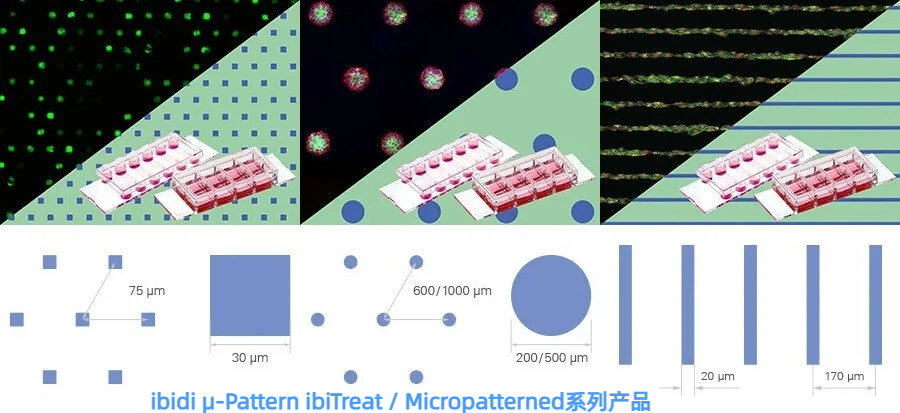
这些技术组合,将体外模型从静态结构转变为动态系统,让细胞与微环境的互作驱动功能发生。
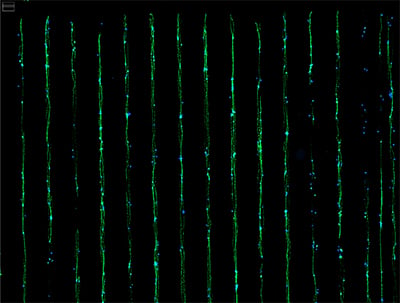
图4.在µ-Slide VI 0.4 µ-Pattern ibiTreat lin20, pit170上培养的人类RealDRG。细胞接种前,载玻片在37°C下用丝素蛋白预包被2小时。细胞培养72小时后,进行固定并用MitoTracker和DAPI染色。图片提供:Moran Amit课题组,MD Anderson Cancer Center,University of Texas
不存在一个单一、完美的体外神经系统模型。每个系统都捕捉了不同层级的复杂性,从孤立的细胞机制到类组织结构和受控的相互作用。
真正的力量在于结合这些方法:
• 以2D体系解析机制
• 以3D培养提升生理相关性
• 以动态微环境逼近体内真实条件
使研究者能够构建对神经元生物学更全面的理解。
随着这些技术不断发展,它们不仅在改进我们研究大脑的方式,也在重新定义神经科学研究的无限可能。
[1] Wu Y-Y, et al. Opportunities and challenges for the use of induced pluripotent stem cells in modelling neurodegenerative disease. Open Biology. 2019;9(1).
[2] Zhu H, et al. Recent advances in 3D models of the nervous system for neural regeneration research and drug development. Acta Biomaterialia. 2025;202:1-26.
[3] Menduti G, Boido M. Recent Advances in High-Content Imaging and Analysis in iPSC-Based Modelling of Neurodegenerative Diseases. Int J Mol Sci. 2023;24(19).
[4] Zehtabian A, et al. Automated Analysis of Neuronal Morphology in 2D Fluorescence Micrographs through an Unsupervised Semantic Segmentation of Neurons. Neuroscience. 2024;551:333-344.
[5] Li Y, et al. Advances and Applications of Brain Organoids. Neurosci Bull. 2023;39(11):1703-1716.
[6] Bose R, Banerjee S, Dunbar GL. Modeling Neurological Disorders in 3D Organoids Using Human-Derived Pluripotent Stem Cells. Front Cell Dev Biol. 2021;9:640212.
[7] Oddo A, et al. Advances in Microfluidic Blood-Brain Barrier Models. Trends Biotechnol. 2019;37(12):1295-1314.
ICP备案号:
沪ICP备15057650号-1
 沪公网安备31011202005471
沪公网安备31011202005471
雷萌生物科技(上海)有限公司 保留所有版权.