date:2011-09-15 00:00:00
胰岛移植是一种新的糖尿病治疗方法,胰岛移植成功的关键在于从供体中分离出纯度高、数量多、活力强的胰岛细胞。胰岛分离技术经历了纯手工分离、半自动分离、全自动控制分离的过程。通过对胰岛细胞分离过程的温度、时间、灌注压力的准确控制和胰岛细胞纯化技术的不断改进,胰岛细胞分离效果将会更好,胰岛移植的成功率也将更高。
1.前言
糖尿病发病率在世界范围内呈明显上升趋势,世界卫生组织公布的数据显示:目前全世界逾2.2亿人患有糖尿病,预计到2030年全世界糖尿病患者将达到3.66亿。中国糖尿病流行病学调查结果表明:在年龄≥20岁的中国人群中,糖尿病和糖尿病前期患病率分别高达9.7%和15.5%,以此推算目前中国有9240万成年人患有糖尿病,有1.48亿人处于糖尿病前期。由于糖尿病是一种终身疾病,它发病率高、并发症较多,其致死率仅次于癌症及心血管疾病,已被世界卫生组织列为危害人类健康的第三大疾病。
糖尿病的治疗方法主要有饮食控制、体育锻炼、药物治疗、胰岛素注射、胰腺器官移植和胰岛细胞移植。饮食控制、体育锻炼、药物与胰岛素注射治疗都无法避免糖尿病并发症的发生,胰腺移植手术风险大、并发症多,还受到供体短缺、免疫排斥等限制,因此这些治疗方法都不是理想的治疗糖尿病方法。
2.胰岛移植的发展
2000年,加拿大Edmonton Alberta University的James Shapiro领导的研究小组探索的胰岛移植方案(Edmonton方案)取得了重大成功。在截至2004年11月按照Edmonton方案接受胰岛移植的47例糖尿病病人中,接受胰岛移植1年后约87%的病人可以完全脱离胰岛素治疗;移植后2年时仍有60%的病人不需要使用胰岛素治疗。实验表明,胰岛移植是治疗胰岛素依赖型糖尿病的有效方法,胰岛移植不仅能够纠正糖代谢的紊乱,而且能够防止或逆转糖尿病的微血管病变。这使胰岛移植成为治疗糖尿病的发展趋势。
3.胰岛细胞分离对胰岛移植的影响
从供体中分离出纯度高、数量多、活力强的胰岛细胞是进行胰岛细胞移植的先决条件。在Edmonton胰岛细胞移植控制组的患者平均需要移植857318个胰岛,从胰岛细胞的数量上也就是说,每例患者需要移植至少2个胰腺的胰岛细胞,所以移植的胰岛细胞的数量和质量都是成功的关键。
4.胰岛细胞分离技术的研究与发展
早在1892年,Minkowski和Von Merin对动物进行胰腺移植实验。实验结果显示:经全胰切除手术后将部分胰腺组织植于皮下(不与消化系统相连)的实验犬虽然仍会出现糖尿病,但其死亡率低于单纯全胰腺切除的对照组。虽然没有进行胰岛细胞分离,直接将全胰植于皮下,但其对糖尿病的治疗也起到了一定的效果。
1967年,Lacy用胶原酶震荡消化分离法从大鼠的胰腺中分离出胰岛细胞,胰岛细胞中包括胰岛素分泌细胞。1976年他在啮齿动物模型上完成了胰岛移植,并证实了这一方法治疗糖尿病的可行性。但是这种胰岛分离和移植方法的部分步骤比较繁杂,胰腺的灌注、消化、胰岛细胞分离全部采用人工控制,分离过程技术性强,需要较长的熟练过程,对胰岛的破坏性较大。
上世纪70年代,Ficoll从外分泌腺成功分离人胰岛细胞。1986年,圣路易斯研究组的Ricordi发展半自动酶解和胰腺收集的方法,在消化室内采用循环蠕动泵对供体胰腺进行循环灌注,并用双硫腙染色监测游离胰岛消化过程,既减少了胶原酶用量,缩短了分离时间,同时减少了机械损伤及污染的机会。而在胰岛分离剂的选用上,因为用Euro-Ficoll梯度进行胰岛纯化过程,胰岛及腺外分泌组织的稳定性改善,使二者较好地分开,而且能较好地恢复胰岛的活力,使胰岛细胞移植成为可能。
1996年,Shapiro提出了一种改良型静止消化技术,并将其与标准化组织切碎消化技术进行了严格的双盲比较,结果显示胆总管内胶原酶注射静止法胰岛产量高出切碎法47.5%,且胰岛功能保留方面亦优于切碎法。
90年代中末期,Roche公司商品化的混合性胶原酶和蛋白酶-Liberase用于临床胰岛分离,以及COBE2991细胞分离仪的应用显著地改善了胰岛消化后的纯化过程,大大提高了用于移植的胰岛的纯度。
2000年Edmonton方案取得了巨大成功,Edmonton实验方案中采用的灌注和消化方法是:在4℃的温度下对供体胰腺在胰腺修整盘内进行必要的修整;胰腺的灌注装置见图1,将合适管径的聚乙烯管,经胰腺乳头部的主胰管或横断胰腺上的主胰管插入,并结扎固定于胰管上。经主胰管插管灌注复合胶原酶溶液,充分灌注胰腺。复合胶原酶灌注完毕,再进行消化,消化装置见图2,将胰腺剪切成5-6块,放入消化罐中,于37℃下机械震荡消化,并在消化一定时间后抽取样品进行监测,当检测到样品中游离胰岛数量超过50%,并且可以看到有>200μm的游离胰岛时,终止消化过程。
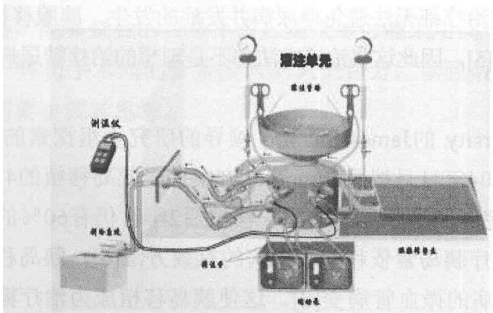
图1
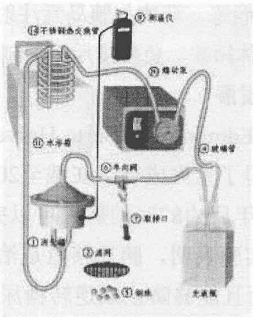
图2
2011年,浙江大学医学院附属第一医院的冯靖祎、胡亮对胰岛干细胞分离过程的温度控制进行了深入的研究,研制了采用单片机控制、半导体变温的胰岛细胞分离全程温度控制系统。该系统通过对胰岛干细胞分离过程的温度的准确控制,提高了胰岛细胞分离的数量和质量。
目前,美国Biorep 公司推出的生物流体灌注设备和胰岛分离机,通过软件控制供体胰腺的灌注和消化的压力、温度、时间,从而实现供体胰腺的灌注和消化过程的自动控制。其操作流程如图3。全自动胰腺灌注消化纯化设备在胰岛分离过程的广泛应用推动了胰岛细胞分离技术的发展,进而推动了胰岛细胞移植的发展。
5.展望
总之,成人胰岛细胞移植作为治疗糖尿病的一种新方法,已经展现出广阔的临床应用前景及巨大的社会与经济效益。随着胰岛细胞分离纯化技术的进一步改善,从供体中分离出胰岛细胞将会数量更多、活性更高、质量更好,胰岛细胞移植的成功率也将得到进一步提升,进而使胰岛细胞移植术更广泛地应用于糖尿病治疗。
ICP备案号:
沪ICP备15057650号-1
 沪公网安备31011202005471
沪公网安备31011202005471
雷萌生物科技(上海)有限公司 保留所有版权.